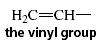Turinys
Alkenai
Bendra formulė
Molekulės struktūra
- Alkenams būdinga
hibridizacija:
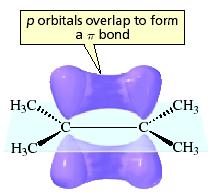
- Dvigubą jungtį sudaro dviejų tipų ryšiai: σ ir π.
- π ryšys susidaro susiglaudžiant nehibridizuotoms p orbitalėms. Kadangi elektronų debesys persidengia nedaug, ryšys yra žymiai silpnesnis, taigi jį ir lengviau nutraukti.
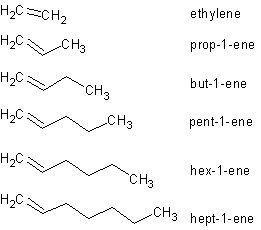
Eteno homologinė eilė
Izomerija
Alkenams būdinga:
- Grandinės izomerija (žr. alkanus).
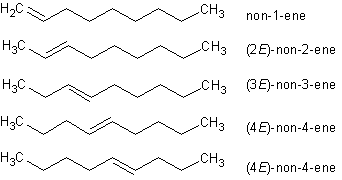
- Dvigubo ryšio padėties izomerija:
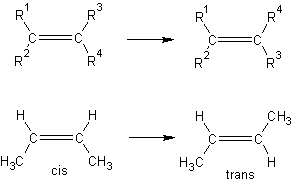
- Geometrinė cis-trans izomerija:
π ryšys tam tikromis sąlygomis gali nutrūkti ir tada atsiranda tikimybė molekulei apsisukti aplink dvigubąjį ryšį. Jei prie dvigubą ryšį sudarančių anglių yra skirtingi pakaitai, susidarys naujas junginys, turintis šiek tiek kitokias savybes. Jei vienodi pakaitai yra vienoje plokštumoje, izomeras vadinamas cis-izomeru, o jei skirtingose - trans-izomeru.
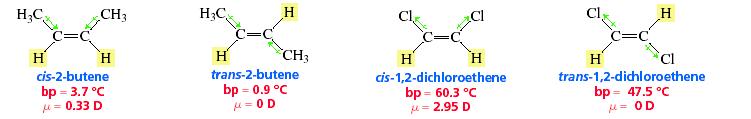
cis-trans izomerai skiriasi savo cheminėmis savybėmis:
Nomenklatūra
Dvigubą ryšį nusako pavadinimo galūnė -enas.
Fizikinės savybės
Labai silpnai polinės molekulės. Pirmi trys eteno homologinės eilės nariai yra dujos, iki C18 - skysčiai, toliau kietosios medžiagos. Fzikinės savybės labai panašios į alkanų. Gerai tirpsta nepoliniuose tirpikliuose. Vandenyje - ne.
Jei nenurodyta kitaip, šio wiki turinys ginamas tokia licencija: CC Attribution-Noncommercial-Share Alike 4.0 International